研究プロジェクト
- HOME
- 研究プロジェクト
- クロマチン制御因子の小脳発生と髄芽腫形成における役割の解析
- 脳腫瘍特異的な融合遺伝子の発がん機能の解析
- 脳腫瘍と脳内微小環境の新研究
- アルツハイマー病発症機構におけるアミロイド蓄積およびAβ代謝(産生・分解)制御メカニズムの解明
- 小児がんにおける染色体外DNA
- 未分化多形肉腫の遺伝的多様性
川内
クロマチン制御因子の小脳発生と髄芽腫形成における役割の解析
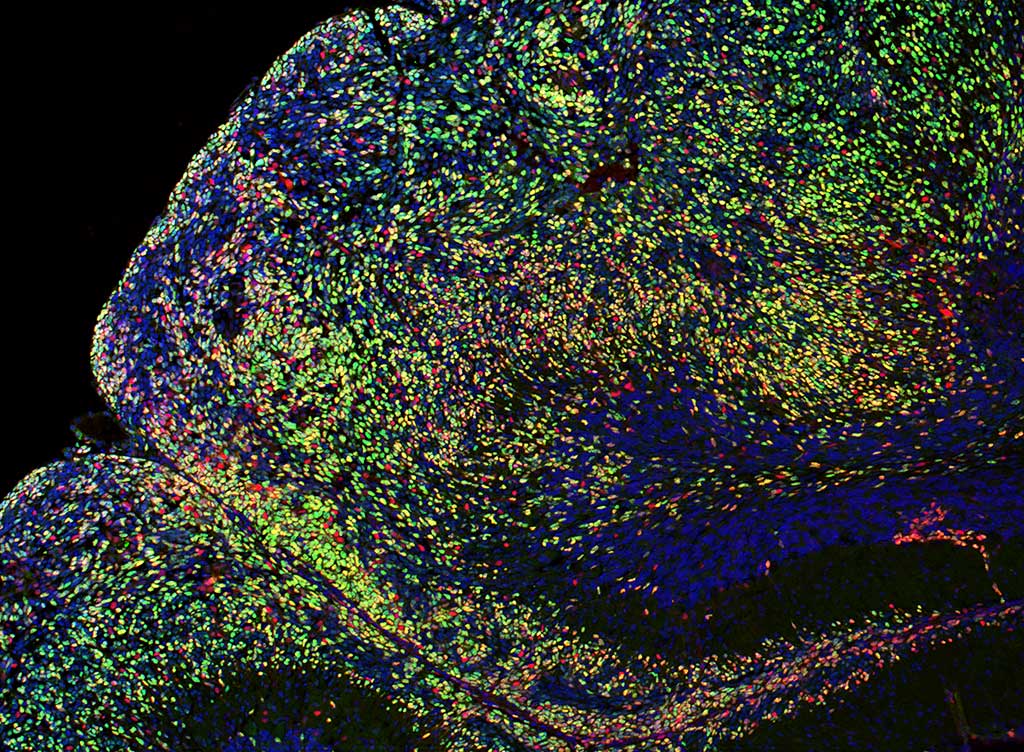
近年、次世代シーケンス技術の発展によって、小児脳腫瘍のひとつである髄芽腫(ずいがしゅ)の分子レベルでの理解が大きく進んできました。特に、髄芽腫ではクロマチン制御因子(=DNAの折りたたみ構造を調節するタンパク質)の変異がよく見られ、これによりエピゲノム(遺伝子の使われ方)が変化していることがわかっています。
しかし、こうした変異が実際にどのように腫瘍の発生や進展に関わっているのか、その仕組みはまだ十分に解明されていません。
そこで本研究では、マウスの遺伝学的手法やCRISPRなどのゲノム編集技術を用いて、まずはクロマチン制御因子が正常な小脳の発生においてどのような役割を果たしているのかを明らかにします。さらに、それらの因子に変異が入ったときにどのような変化が起きて腫瘍が形成されるのかを解析することで、がん発生の新しいメカニズムの理解を目指しています。
このような研究は、「がんの設計図」だけでなく「がんの設計図の読み方(エピゲノム)」に注目するという、新しい視点からのアプローチであり、将来的にはがんの分子特性に応じた治療法の開発にもつながると期待されています。
参考原著論文: Zuckermann et al. Nat Commun. 2015; Feng et al. Nat Commun. 2017; Kutcher et al. Genes Dev. 2020; Shiraishi et al. Dev Cell 2024; Wang et al. Cell Rep 2025
脳腫瘍特異的な融合遺伝子の発がん機能の解析
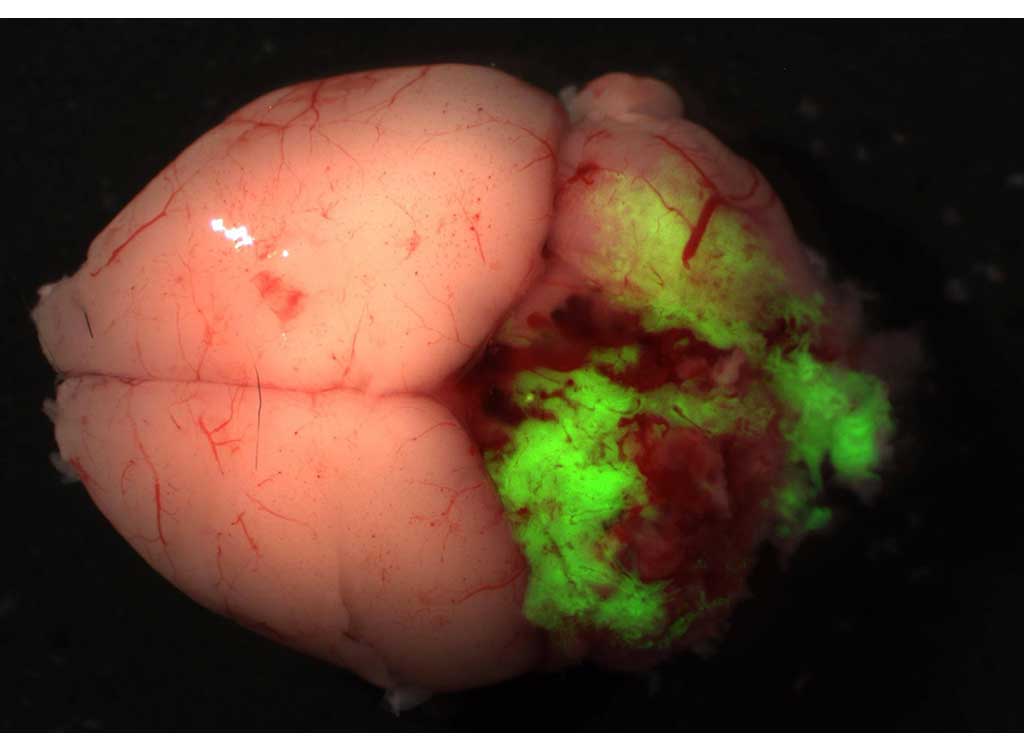
がん細胞では、ときに本来は別々に存在している2つの遺伝子が、ゲノムの異常によってつながり、融合遺伝子と呼ばれる新しい遺伝子がつくられることがあります。
この融合遺伝子は正常な細胞では見られず、がんに特異的な性質を持ち、がんの発生や進展を引き起こす強力なドライバーになることが知られています。
特に小児脳腫瘍では、このような融合遺伝子が重要な役割を果たすことが近年注目されており、2016年に米国で発表されたBlue Ribbon Panelでも、融合遺伝子の研究は小児がんの理解における最優先課題の一つとされました。
私たちの研究では、小児脳腫瘍に特異的に発現する融合遺伝子に注目し、それが腫瘍形成にどのように関与しているのか、またどのようながん特有のシグナル伝達経路を引き起こしているのかを、生体内モデルを用いて明らかにしています。
さらに私たちの成果は、世界保健機関(WHO)による脳腫瘍の最新の分子分類(2021年改訂)にも反映されており、特定の融合遺伝子の存在が、上衣腫のサブグループを定義する上での新たな指標となることを示しました。これは、腫瘍の診断・分類・治療方針の決定において非常に重要な意味を持ちます。
このように、脳腫瘍のさまざまな融合遺伝子の分子機構を理解することで、がんの本質的な性質に迫り、精密医療(Precision Medicine)へとつながる新たな治療戦略の開発を目指しています。
参考原著論文: Pajtler et al. Nat Commun. 2019; Zheng et al. Cancer Discov. 2021
脳腫瘍と脳内微小環境の新研究
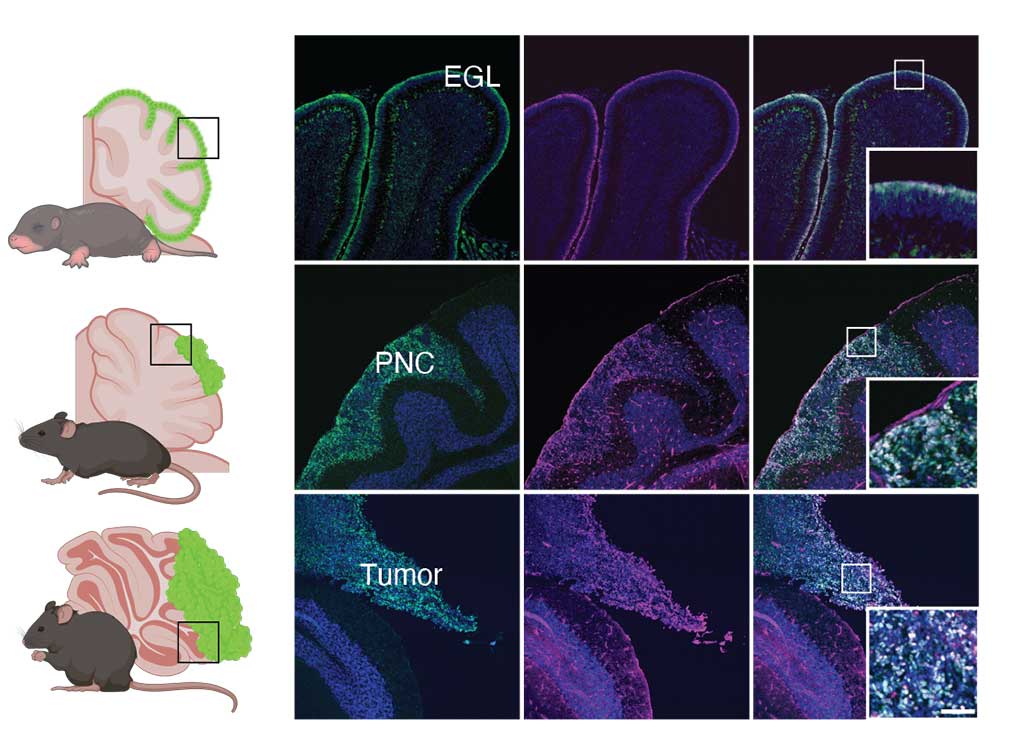
細胞を巻き込みながら、自分にとって有利な環境を作り出すという、非常に巧妙な性質を持っています。
そしてこの性質は、脳腫瘍でも例外ではありません。最近の研究では、脳腫瘍が周囲の神経細胞やグリア細胞と複雑に関わり合いながら、「がんにとって居心地の良い環境」=脳特有の微小環境ネットワークを構築していることが明らかになってきました。
こうしたネットワークが、がんの進展や悪性化を後押ししていると考えられています。しかし、その仕組みを理解するためには、生体内に近い状態でがんがどのように広がっていくのかを観察することが重要です。
私たちの研究室では、これまでに独自に開発してきた小児脳腫瘍モデルを活用し、がんと脳細胞との相互作用の仕組みを詳しく調べています。さらに現在は、
-
東京科学大学の上阪直史教授(神経回路解析)
-
フランス・キュリー研究所のOlivier Ayrault博士(小児脳腫瘍の分子生物学)
との国際共同研究を通じて、
「ヒトの腫瘍サンプルを使ったオミクス解析」と
「マウスを用いた腫瘍モデル」、
そして「神経科学の知見」を組み合わせた、新しい学際的な研究分野を切り開いています。
このような研究は、がんを“脳の中で生きている生き物”としてとらえ直すことで、これまでにない視点から新しい治療戦略を見出すことにつながると期待されています。
参考原著論文: Forget et al. Cancer Cell 2018
鄒
アルツハイマー病発症機構におけるアミロイド蓄積およびAβ代謝(産生・分解)制御メカニズムの解明
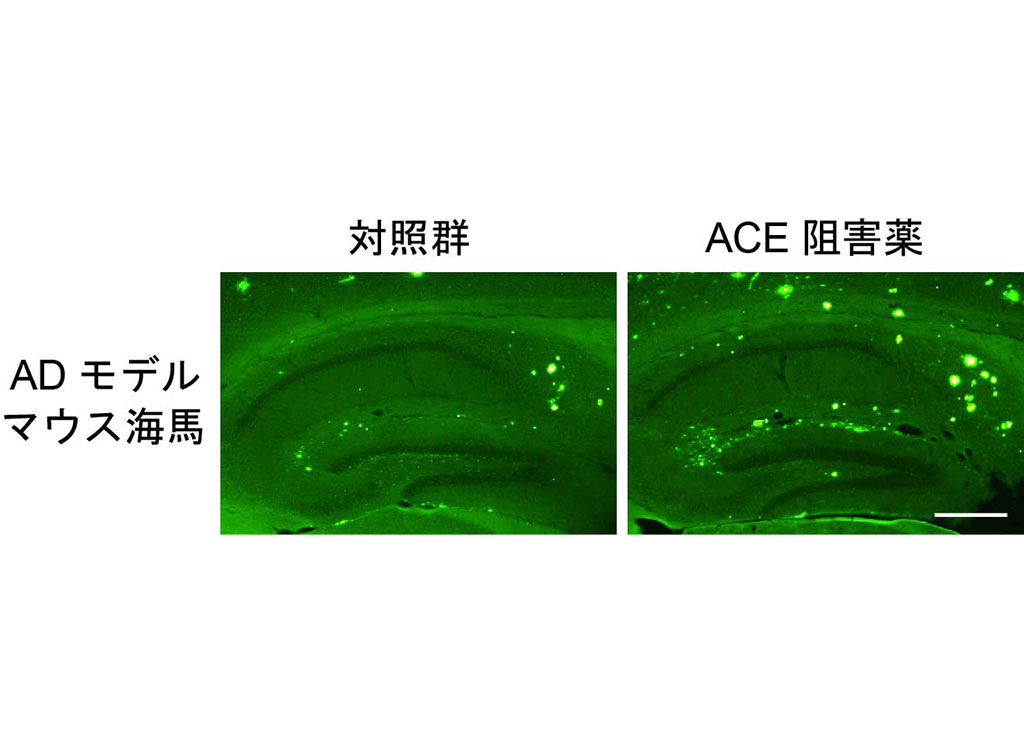
超高齢社会に突入した日本では、認知症患者数は増加の一途をたどり、特に認知症の60%前後を占めるとされるアルツハイマー病の予防・治療法の確立は、急務です。我々のチームでは、アルツハイマー病をはじめとする神経変性疾患の病態解明を行い、分子メカニズムに介入する形で予防・治療法解明のための研究を行っています。
(1)アルツハイマー病の発症には、アミロイドβ蛋白(Aβ)の脳内蓄積が深くかかわっていると考えられています。我々は、世界に先駆けてAβ42は強い毒性を発揮するが、Aβ40は神経保護作用を持つことを見出しました。すなわち、(i) Aβ42は強い凝集性を持つため神経毒性を発揮するが、単体で存在しうるAβ40は遷移金属をキレートして活性酸素の発生を抑制し、活性酸素による神経細胞死を抑制し、(ii) 単体Aβ40はAβ42と結合することにより、Aβ42のβ-sheet形成を阻害し、Aβ42の重合体形成・線維化を抑制します。その結果、単体Aβ40には、Aβ42のもつ神経毒性を抑制する作用があることを明らかになりました。
チャップマン
小児がんにおける染色体外DNA
染色体外DNA(ecDNA、ダブルミニッツとも呼ばれる)は、多くのヒトがんに生じる、メガベース規模の円形局所ゲノムDNA増幅である。ecDNA配列には一般に、選択的な適応上の 優位性をもたらす癌遺伝子またはその他の機能的要素が含まれており、セントロメアを欠くため、細胞分裂時の不均等な分配および腫瘍内不均一性を引き起こす。コピー数の不均一性と 正の選択の強力な組み合わせが、高コピー数の癌遺伝子増幅、急速な腫瘍進化、および治療抵抗性を促進する。
ペアエンド全ゲノムシークエンシングは、ecDNA上に取り込まれた癌遺伝子やその他の配列を同定するための、費用対効果が高く効率的な手法として台頭してきた。初期の小児 パンキャンサーゲノム研究では大部分が見過ごされていたが、近年の研究により、様々な成人がんおよび一部の小児がん種におけるecDNAの 頻度が明らかにされてきた。小児がんは 成人がんと比較してソマティック変異頻度が14倍低く、固有のドライバー変異や増幅を有することを踏まえ、我々は現在、幅広い一次および再発小児がんにわたるecDNAの頻度とその 生存との関連を検討している。
参考原著論文: Chapman et al. medRxiv 2025; Chapman et al. Nature Genetics 2023
未分化多形肉腫の遺伝的多様性
未分化多形肉腫(UPS)は、一部の腫瘍において散発的な局所増幅を伴い、予後も様々である、定義が不明確な腫瘍診断である。遺伝的不均一性と有効な分子標的療法の欠如は、 新たな臨床的に実用可能なバイオマーカーを同定する必要性を浮き彫りにしている。本プロジェクトは、約50例のUPS腫瘍および対応する患者由来異種移植モデル(PDX)を対象に、 以下を目的とする:
- UPSおよび関連肉腫の遺伝的・後成遺伝学的・転写的多様性を網羅的に解析する;
- ecDNA陽性UPS腫瘍を同定し、ecDNAと患者アウトカムとの関連の可能性を検討する;および
- ゲノム情報を活用した新たな予後予測および治療戦略を検討する。